Logam cenderung memiliki titik leleh dan titik didih yang tinggi sehingga memberikan kesan kuatnya ikatan yang terjadi antara atom-atomnya. Secara rata-rata logam seperti natrium (titik leleh 97.8°C) meleleh pada suhu yang sangat jauh lebih tinggi dibanding unsur (neon) yang mendahuluinya pada tabel periodik.
Unsur logam mempunyai sedit elektron valensi sehingga elektron dapat bergerak bebas dan berpindah dari satu atom ke atom lain. Mobilitas elektron dalam logam sedemikian bebas sehingga elektron valensi mengalami delokalisasi, yaitu suatu keadaan di mana elektron valensi tidak tetap posisinya pada satu atom, tetapi senantiasa berpindah-pindah dari satu atom ke atom lain. Logam terikat bersamaan melalui kekuatan dayatarik yang kuat antara inti positif dengan elektron yang terdelokalisasi seperti gambar berikut :
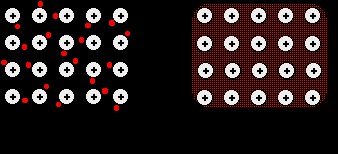
Hal ini kadang-kandang dilukisakan sebagai “susunan inti positif di lautan elektron” karena elektron-elektron valensi berbaur menyerupai awan atau lautan yang membungkus ion-ion positif logam di dalamnya.
Ikatan ini adalah ikatan antar logam dalam bentuk atom (bukan ion).
Struktur logam tersebut dapat menjelaskan sifat-sifat khas logam, seperti daya hantar listrik dan sifat dapat ditempa. Logam adalah konduktor yang baik karena elektron valensinya mudah mengalir. Logam dapat ditempa karena ketika logam dipukul atau ditarik, atom-atom logam hanya bergeser sedangkan ikatan di antaranya tidah terputus.













