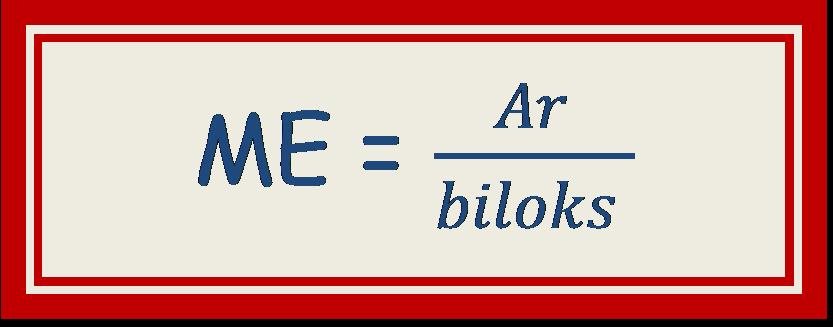Kita pasti pernah melihat atau memakai perhiasan seperti cincin, kalung atau gelang. Umumnya perhiasan yang dikenakan terbuat dari logam yang mempunyai daya pantul yang tinggi terhadap cahaya sehingga terlihat kilau dari perhiasan tersebut. Logam yang dipakai biasanya perak(Ag) dan emas(Au).
Logam emas murni mempunyai harga yang cukup mahal. Bagi kalangan menengah ke atas memang tidak menjadi masalah, tetapi bagaimana jika orang yang tidak ingin mengeluarkan biaya tinggi untuk sebuah perhiasan, cara yang digunakan ialah dengan cara penyepuhan, emas tersebut dapat dilapiskan ke permukaan logam lain. Walaupun tidak setara dengan emas murni atau campuran emas, secasa sepintas akan terlihat seperti emas. Dengan demikian harga dari sebuah pehiasan dapat lebih terjangkau.
Pada proses penyepuhan ini, larutan elektrolit yang digunakan adalah emas klorida (AuCl3), dengan emas sebagai anodanya, sedangkan katodanya adalah tembaga. Pada katoda akan terjadi pengendapan emas, sedangkan pada anoda emas terus menerus larut. Endapan yang dihasilkan dari proses elektrolisis ini dapat kita hitung massanya dengan menggunakan perhitungan dalam hukum Faraday.
Pada tahun 1831-1832, jauh sebelum penemuan elektron, Michael Faraday dari Inggris, telah menemukan hubungan kuantitatif antara massa zat yang dibebaskan pada elektrolisis dengan jumlah listrik yang digunakan. Penemuan ini disimpulkannya dalam dua hukum berikut.
Hukum Faraday 1:
“Massa zat yang dibebaskan pada elektrolisis (G) berbanding lurus dengan jumlah listrik yang digunakan (Q)”.
G ≈ Q …… (1.1)
Jumlah muatan listrik (Q) sama dengan hasil kali dari kuat arus (i) dengan waktu (t).
Q = i x t ………(1.2)
Jadi, persamaan (1.1) di atas dapat dituliskan sebagai berikut.
G i × t ………(1.3)

Jika jumlah listrik yang sama dialirkan ke dalam dua atau lebih sel elektrolisis yang berbeda maka perbandingan massa zat yang dibebaskan sama dengan perbandingan massa ekuivalennya.
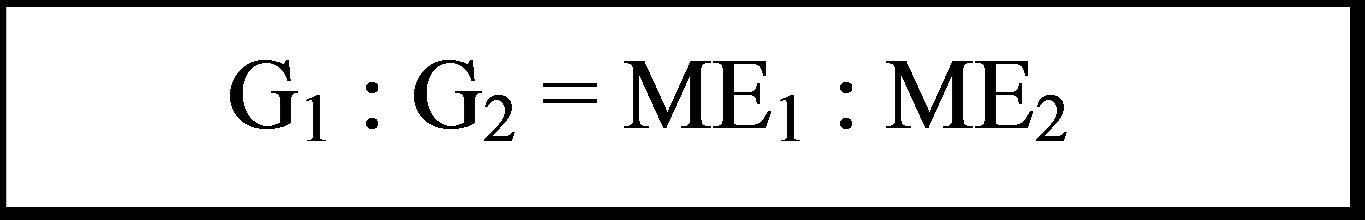
Dimana:
G = massa zat (gram)
ME = beret ekivalen = Ar/Valensi = Mr/Valensi
Penggabungan hukum Faraday I dan II menghasilkan persamaan baru sebagai berikut.

(k = tetapan yang ditemukan Faraday yaitu sebesar 1/96500)
Jadi, untuk mencari berat zat yang dihasilkan pada proses elektrolisis dapat menggunakan persamaan berikut.

Dengan,
G = massa zat yang dihasilkan (dalam gram)
i = kuat arus (dalam ampere)
t = waktu (dalam detik)
ME = massa ekuivalen
Massa ekivalen dari unsur-unsur logam sama dengan massa atom relative (Ar) dibagi dengan bilangan oksidasinya (biloks)