Ada 4 jenis sifat keperiodikan unsur yang dipelajari di kelas X SMA. yaitu; jari-jari atom, energi ionisasi, afinitas elektron, dan keelektronegatifan.
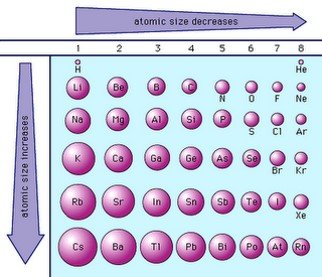
1)Jari-jari atom
Jari-jari atom adalah jarak dari inti atom ke kulit terluar. Para ahli merumuskan jari-jari atom sebagai setengah jarak antara dua inti atom sejenis. Dalam satu periode, jari-jari atom semakin kecil dari kiri ke kanan. Hal ini dikarenakan muatan inti bertambah positif sementara elektron-elektron yang jumlahnya bertambah masih menempati kulit yang sama. Keadaan ini menyebabkan gaya tarik-menarik inti terhadap elektron semakin kuat. Dalam satu golongan, jari-jari atom semakin besar dari atas ke bawah. Hal ini dikarenakan meski muatan inti bertambah positif, namun jumlah kulit semakin banyak. Keadaan ini menyebabkan gaya tarik menarik inti terhadap elektron semakin lemah.
2)Energi ionisasi
Energi ionisasi adalah energi yang dibutuhkan untuk melepaskan satu elektron terluar dari atom atau ion dalam fase gas. Dalam satu periode, energi ionisasi semakin besar dari kiri ke kanan. Hal ini dikarenakan muatan inti bertambah positif dan jari-jari atom berkurang, sehingga gaya tarik menarik inti terhadap elektron terluar semakin kuat. Dalam satu golongan, energi ionisasi semakin kecil dari atas ke bawah. Hal ini dikarenakan meski muatan inti bertambah positif, namun jari-jari atom bertambah besar. Keadaan ini menyebabkan gaya tarik menarik inti terhadap elektron terluar semakin lemah.
3)Afinitas Elektron
Afinitas elektron adalah energi yang terlibat jika suatu atom atau ion dalam fase gas menerima satu elektron membentuk ion negatif (atom bermuatan negatif). Dalam satu periode, afinitas elektron cenderung semakin besar dari kiri ke kanan. Hal ini dikarenakan muatan inti bertambah positif dan jari-jari atom berkurang. Keadaan ini menyebabkan gaya tarik menarik inti terhadap elektron yang ditambahkan akan semakin kuat. Dalam satu golongan, afinitas elektron cenderung semakin kecil dari atas ke bawah. Hal ini dikarenakan meski muatan inti bertambah positif, namun jumlah elektron di kulit dalam semakin banyak. Keadaan ini menyebabkan gaya tarik menarik inti terhadap elektron yang ditambahkan semakin lemah.
4) Keelektronegatifan
Keelektronegatifan (elektronegativitas) adalah suatu ukuran kemampuan atom untuk menarik elektron dalam suatu ikatan kimia. Dalam satu periode, keelektronegatifan semakin besar dari kiri ke kanan. Hal ini dikarenakan muatan inti bertambah positif dan jari-jari atom berkurang, sehingga gaya tarik menarik inti terhadap elektron ikatan semakin kuat. Dalam satu golongan, keelektronegatifan semakin kecil dari atas ke bawah. Hal ini dikarenakan muatan inti bertambah positif, namun jumlah kulit semakin banyak. Akibatnya kemampuan inti untuk menarik elektron ikatan menjadi lemah.