Pada umumnya atom tidak dalam keadaan bebas tetapi bergabung dengan atom lain membentuk senyawa/molekul. Atom-atom memiliki kecenderungan saling bereaksi untuk mencapai konfigurasi elektron stabil yang menyerupai konfigurasi elektron atom-atom gas mulia, yaitu delapan elektron pada kulit terluar. Kecenderungan inilah yang menyebabkan atom-atom berikatan satu dengan lainnya. Ikatan yang terjadi mengakibatkan terjadinya gaya tarik antar atom. Gaya tarik yang mengikat atom-atom disebut ikatan kimia. Pembentukan ikatan bergantung pada keadaan elektron valensi dari atom-atom yang berikatan untuk bergabung membentuk molekul.
Pembentukan molekul dapat terjadi dengan cara transfer elektron atau pemakaian elektron secara bersama-sama pada kulit terluar. Jenis dan kekuatan ikatan yang terjadi sangat menentukan sifat molekul yang terbentuk. Seorang ahli kimia dari Amerika serikat, yaitu Gilbert Newton Lewis (1875 – 1946) dan Albrecht Kosel dari Jerman (1853 – 1972) menerangkan tentang konsep ikatan kimia. Unsur-unsur gas mulia (golongan 8A/18) sukar membentuk senyawa karena konfigurasi elektronnya memiliki susunan elektron yang stabil. Setiap unsur berusaha memiliki konfigurasi elektron seperti yang dimiliki oleh unsur gas mulia, yaitu dengan cara melepaskan elektron atau menangkap elektron. Kecenderungan atom-atom unsur untuk memiliki delapan elektron di kulit terluar disebut kaidah oktet.
Jenis- jenis Ikatan Kimia
Ikatan kimia terbentuk karena atom cenderung membentuk struktur elektron stabil. Ikatan kimia digolongkan menjadi ikatan ion, ikatan kovalen, dan ikatan logam.
a. Ikatan Ion
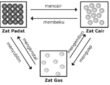
Ikatan ion terbentuk jika terjadi transfer elektron antar atom-atom yang berikatan. Atom yang melepas elektron menjadi ion positif. Atom yang menerima elektron menjadi ion negatif. Muatan yang berlawanan ini menyebabkan ion-ion tersebut saling tarik menarik. Ikatan ion juga dikenal sebagai ikatan elektrovalen.
b. Ikatan Kovalen dan Jenis Ikatan Kovalen
Gas-gas yang kita temukan di alam, seperti hidrogen, nitrogen, oksigen, berada dalam bentuk molekulnya: H2, N2, dan O2. Sebagai atom tunggal, unsur-unsur ini sangat reaktif, sehingga membentuk molekul untuk mencapai konfigurasi elektron yang stabil. Contohnya adalah molekul hidrogen (H2). Atom H hanya mempunyai 1 e-, perlu tambahan 1 e- agar menjadi seperti He. Jika 2 atom H berdekatan, keduanya dapat menggunakan 2 e- yang ada secara bersama, sehingga masing-masing atom H menjadi seperti He. 2 e- tersebut menarik kedua atom H untuk berikatan menjadi molekul H2. Ikatan yang terbentuk adalah ikatan kovalen. Pada ikatan kovalen tidak terjadi transfer elektron, tetapi atom-atomnya menggunakan pasangan elektron valensinya bersama-sama. Ikatan kovalen biasanya digambarkan dengan titik-titik yang mewakili pasangan elektron yang digunakan bersama, atau dengan suatu garis.
c. Ikatan Logam
Kawat tembaga digunakan sebagai penghantar listrik dalam kabel, besi digunakan untuk setrika sebagai penghantar panas, dan emas atau perakdigunakan untuk perhiasan dalam bentuk yang indah. Apa penyebab logam memiliki sifat tersebut? Hal ini disebabkan atom- atom pada logam tersebut tidak berdiri sendiri-sendiri tetapi bergabung melalui ikatan logam.