Senyawa yang terdapat di alam maupun senyawa buatan diberi nama dengan aturan-aturan tertentu. Tata nama senyawa diatur oleh badan internasional IUPAC (International Union and Pure Applied Chemistry). Nama suatu senyawa kimia berkaitan dengan rumus kimia dari senyawa tersebut,misalnya
NaCl : natrium klorida (garam dapur)
CaCl2 : kalsium klorida
MgO : magnesium oksida
CO2 : karbon dioksida (gas asam arang)
NaOH : natrium hidroksida (soda kaustik)
A. Tata Nama Senyawa Kovalen Biner
Senyawa biner adalah senyawa yang terbentuk dari dua unsur yang berbeda. Senyawa biner tidak selalu berupa molekul diatomik.
Cl2 : bukan senyawa biner,tetapi merupakan molekul diatomik
BrCl : merupakan senyawa biner dan termasuk molekul diatomik
H2O : merupakan senyawa biner tetapi bukan termasuk molekul diatomik. Merupakan molekul triatomik(terdiri dari 3 atom)
Penulisan Rumus Kimia Senyawa Biner didahului unsur yang lebih elektropositif dan diikuti oleh unsur yang lebih elektronegatif. Contoh:
Senyawa IF3
Keelektronegatifan I = 2,5 (lebih elektropositif)
Keelektronegatifan F = 4,0(lebih elektronegatif)
Karena nilai keelektonegatifan unsur I < unsur F,maka I merupakan unsur yang lebih elektropotif. Sehingga penulisan Rumus Kimianya didahului dengan unsur I lalu diikuti unsur F.
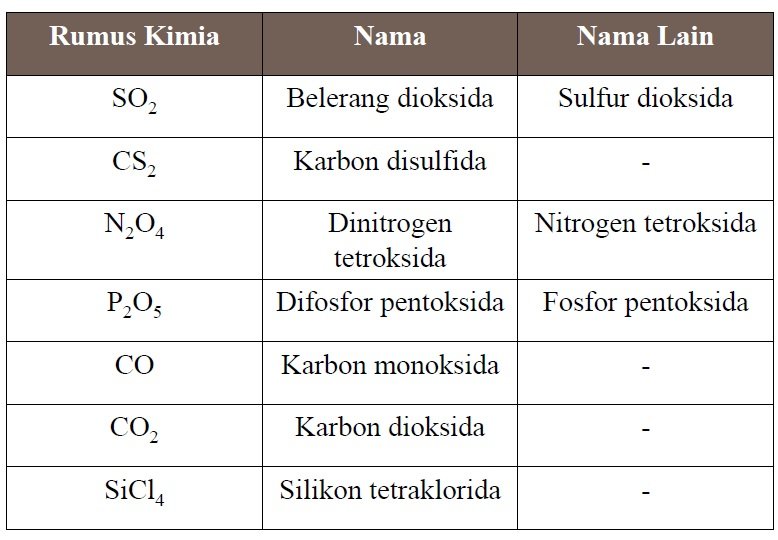
Berikut aturan penamaan senyawa kovalen biner:
•Atom yang di depan disebut sesuai dengan nama unsurnya,diikuti dengan nama unsur berikutnya,dan diberi akhiran –ida
•Jumlah atom(angka subskrip) disebut sebagai awalan dengan menggunakan angka latin
1 = mono
2 = di
3 = tri
4 = tetra
5 = penta
6 = heksa
7 = hepta
8 = okta
9 = nona
10 = deka
Contoh :
SO2
Atom yang berada di depan diberi nama sesuai dengan nama unsurnya. Atom S → nama unsurnya yaitu Belerang. Lalu diikuti unsur dibelakangnya yang diberi akhiran –ida. Atom O → nama unsurnya yaitu Oksigen,diberi akhiran –ida → Oksida. Dalam senyawa terdapat 2 atom O,maka diberi nama Dioksida.
B. Tata Nama Senyawa Ion
Senyawa ion adalah gabungan dari ion positif dan ion negatif. Nama ion positif disebutkan terlebih dahulu baru diikuti nama ion negatifnya.
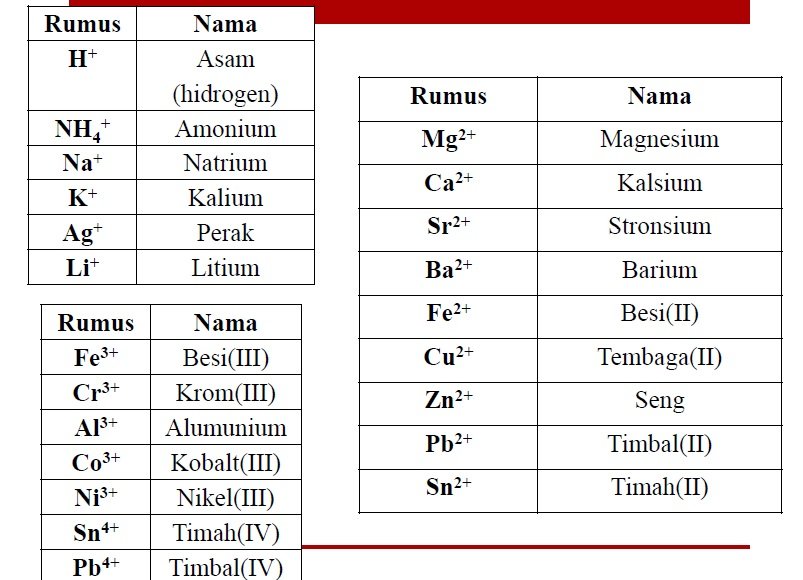
Nama Ion Positif (Kation)
Ion positif terbentuk dari unsur yang melepaskan elektronnya. Unsur tersebut dapat berupa unsur logam (Na+,Fe2+, Fe3+) ataupun unsur non-logam(H+ dan NH4+).
•Unsur-unsur golongan IA, IIA ,dan IIIA → membentuk ion dengan satu muatan
•Unsur-unsur transisi(golongan IIIB – VIIIB serta IB dan IIB) umumnya dapat membentuk ion positif dengan muatan lebih dari satu.
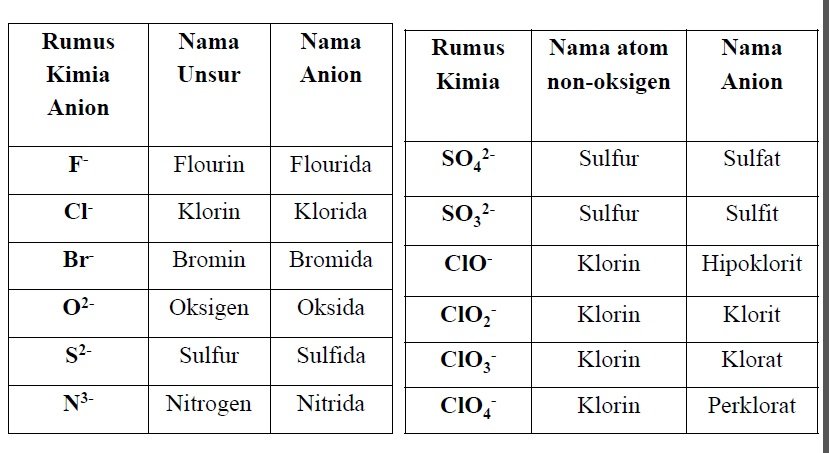
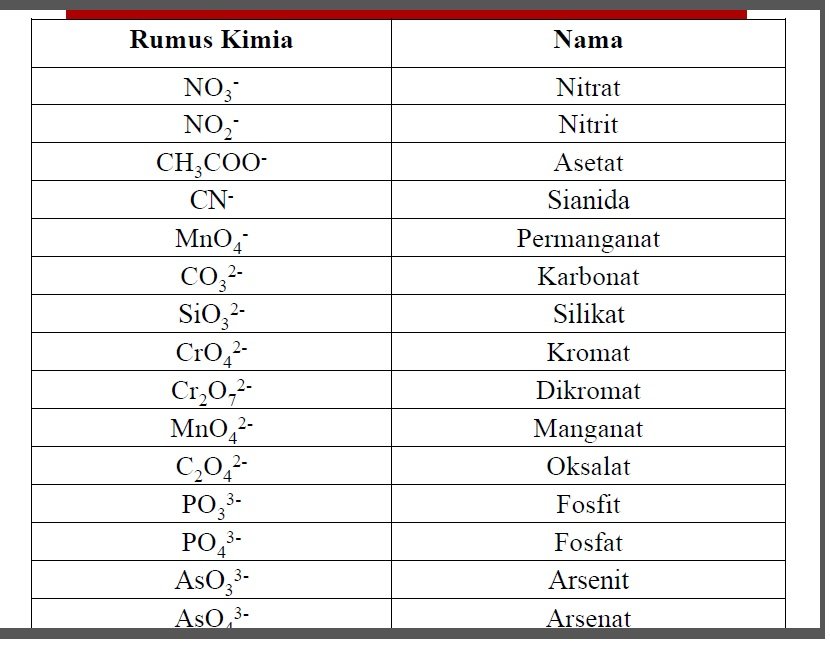
Nama Ion Negatif (Anion)
Ion negatif terbentuk dari sebuah atom (monoatomik) dan beberapa atom (poliatomik).
Contohnya: F-,Cl-,O2-
•Monoatomik → nama unsurnya lalu ditambah dengan akhiran –ida.
•Poliatomik : Mengandung oksigen (ion oksi) → diberi nama atom non-oksigen dan diberi akhiran dengan –at atau –it. Selain itu beberapa ion oksi ada yang diberi awalan per- dan hipo-